Дистилят я ція (від лат. Distillatio - стікання краплями), перегонка, розділення рідких сумішей на різні за складом фракції. Контроль здійснюється шляхом відмінності температур кипіння компонентів суміші. Залежно від фізичних властивостей компонентів рідких сумішей застосовують різні способи Д.
Проста Д. (рис. 1) проводиться частковим випаровуванням киплячій рідкої суміші, безперервним відведенням і подальшою конденсацією пари. Так як пари над киплячою рідкою сумішшю містять низкокипящих компонентів більше, ніж рідина, то конденсат (званий дистилятом) збагачується, а не випарувався, рідина (кубовий залишок) збіднюється ними. У дистиляційному кубі 1 кипить вихідна рідка суміш. Пари, що утворюються безперервно відводяться в конденсатор 2, де утворюється дистилят, який стікає в приймач 3. При простій Д. зміст низькокиплячих компонентів в паровій і рідкій фазах безперервно падає. Тому склад дистиляту міняється в часі. Проста Д., здійснювана за описаною схемою, - періодичний процес. Для прискорення процесу застосовують напівбезперервна Д., при якій в дистиляційний куб безперервно надходить вихідна суміш, рівна масі йдуть парів.
Фракційна Д., звана також дробової перегонкою (рис. 2), - один з різновидів простий Д. Таку Д. застосовують для поділу суміші рідин на фракції, киплячі в вузьких інтервалах температур. При цьому дистиляти різних складів відводять (послідовно в часі) в кілька збірок. До збірки 1 надходить перша за часом порція дистиляту, найбільш багата низькокиплячими компонентами, до збірки 2 - менш багата, до збірки 3 - ще менше багата і т.д. У кожному з цих дистилятів (фракціях) переважає один або кілька компонентів вихідної суміші з близькими температурами кипіння. Просту Д. для поліпшення поділу сумішей часто комбінують з противоточной дефлегмацією (рис. 3). При цьому утворюються в кубі 1 пари частково конденсуються в дефлегматоре 2, конденсат (флегма) безперервно повертається в куб, а залишок парів після дефлегматора поступає в конденсатор 3, звідки дистилят стікає в збірник 4. Цим способом досягається більше збагачення дистиляту низькокиплячими компонентами, тому що при частковій конденсації (дефлегмації) парів переважно конденсуються висококиплячі компоненти.
Рівноважна Д. (одноразове випаровування) характеризується випаровуванням частини рідини і тривалим контактом пари з не випарувався, рідиною до досягнення фазового рівноваги (рис. 4). Колективна суміш проходить по трубах 1, обігрівається зовні топковим газами. Новоутворена при цьому парожидкостная суміш, близька до рівноважного стану, надходить в сепаратор 2 для механічного відділення рідини від пара. Пари (П) з сепаратора поступають в конденсатор, звідки дистилят стікає в приймач, а решта в сепараторі рідина відводиться в збірник. У цьому процесі співвідношення між парою і рідиною визначається матеріальним балансом і умовами фазового рівноваги. Рівноважна Д. рідко застосовується для двокомпонентних сумішей; хороші результати отримують в основному в разі багатокомпонентних сумішей, з яких можна отримати фракції, сильно розрізняються за складом.
Д. в струмі водяної пари або інертних газів застосовують, коли необхідно знизити температуру процесу відгону, в разі поділу нетермостойкіе компонентів, а також для відгону речовин з низькою температурою випаровування від компонентів з високою температурою випаровування. Бульбашки водяної пари або інертного газу барботируют через шар рідини (див. барботування ). При Д. з водяною парою утворилася суміш парів води і летючого компоненту відводиться з апарату і піддається конденсації і охолодження. Склад утворюються в кубі парів не залежить від складу рідини, а температура кипіння суміші завжди нижча за температуру кипіння кожного з компонентів при даному тиску. При Д. з інертним газом компоненти розчину випаровуються в потік газу, навіть якщо розчин не кипить, а пароутворення при випаровуванні може відбуватися при будь-яких температурах, незалежно від зовнішнього тиску, що дозволяє вести процес при низьких температурах.
Молекулярна Д. заснована на поділі рідких сумішей вільним їх випаровуванням у високому вакуумі 133-13,3 мн / м2 (10-3-10-4 мм рт. Ст.) При температурі нижче точки їх кипіння. Процес проводять при взаємному розташуванні поверхонь випаровування і конденсації на відстані, меншій довжини вільного пробігу молекул речовини, що переганяється. Завдяки вакууму молекули пара рухаються від поверхні, що випаровує до конденсується з мінімальним числом зіткнень. При молекулярної Д. зміна складу пара в порівнянні зі складом рідини визначається різницею швидкостей випаровування компонентів. Тому цим способом можна розділяти суміші, компоненти яких мають однаковий тиском пари. При даній температурі рідини і відповідному їй тиску парів швидкість молекулярної Д. зростає з пониженням тиску в апараті.
Для зменшення часу дифузії молекул летючого компоненту з глибини шару рідини до поверхні випаровування процес в сучасних молекулярних кубах проводять в дуже тонких плівках рідини, що дозволяє, крім того, зменшити час перебування речовини на поверхні випаровування і небезпека його термічного розкладання. Для молекулярної Д. застосовують апарати з горизонтальними і вертикальними поверхнями випаровування, а також отримали найбільше промислове застосування відцентрові апарати. В останніх процес характеризується найменшими товщиною рідкої плівки (в середньому 0,05 мм) і часом її перебування на поверхні нагрівання (0,03-1,2 сек). У відцентрових апаратах (рис. 5) на випарник 1, що представляє собою найшвидше конус (іноді диск), подається суміш, що розділяється. Відцентрова сила переміщує рідина від центру до периферії (вгору). Пари речовини, що переганяється збираються на нерухомому конденсаторі 2, розташованому паралельно поверхні випарника, звідки дистилят безперервно відводиться. Залишок після перегонки скидається в кільцевої жолоб 3 і виводиться з куба. Для збільшення ефекту поділу встановлюють кілька апаратів послідовно.
Молекулярну Д. застосовують для розділення і очищення високомолекулярних і термічно нестійких органічних речовин, наприклад для очищення ефірів себациновой, стеаринової, олеїнової та ін. Кислот, для виділення вітамінів з риб'ячого жиру і різних рослинних масел, при виробництві медичних препаратів, вакуумних масел і ін.
У металургії поняття Д. об'єднує пірометалургічні процеси (див. Пірометалургія ), Засновані на перекладі відновлюваного металу (див. відновлення металів ) В пароподібний стан з подальшою конденсацією. Металургійна Д. - поєднання хімічного (окисно-відновної реакції) і фізичного (випаровування і конденсації) процесів. Відновлення проводять з використанням вуглецевих відновників (див. Карботермія ) Або металотермічним способом (див. Металлотермія ). Можливо виділення вільного металу при окислювальному випалюванні сульфідних концентратів. Ступінь поділу при Д. визначається різницею складу суміші, що переганяється і її пара. Повнота переходу металу в газову фазу при Д. визначається відновленням металів при температурах і тисках, що забезпечують отримання відновленого металу в пароподібному агрегатному стані.
Літ .: Касаткін А. Г., Основні процеси і апарати хімічної технології, 8 видавництво., М., 1971; Гельперин Н. І., Дистиляція і ректифікація, М. - Л., 1947; Багатурія С. А., Теорія і розрахунок перегонки і ректифікації, М., 1961; Ціборовський Я., Процеси хімічної технології, пров. з пол., Л., 1958; Матрозов В. І., Апаратура для молекулярної дистиляції, М., 1954; Чижиков Д. М., Металургія важких кольорових металів, М. - Л., 1948; Лакернік М. М., Електротермія в металургії міді, свинцю і цинку, М., 1964.
В. Л. Пебалк.
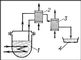
Мал. 3 до ст. Дистиляція.
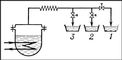
Мал. 2 до ст. Дистиляція.
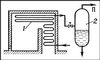
Мал. 4 до ст. Дистиляція.
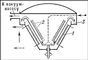
Мал. 5 до ст. Дистиляція.
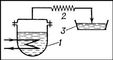
Мал. 1 до ст. Дистиляція.